ou
En continuant, vous acceptez la Politique de confidentialité et les Conditions d'utilisation.
RegAid est entièrement hébergé en Suisse et respecte à la fois le Règlement Général sur la Protection des Données (RGPD) de l'UE et la Loi fédérale suisse sur la Protection des Données (LPD). Toutes les données sont traitées et stockées dans des centres de données suisses. Les données des utilisateurs ne sont jamais utilisées pour l'entraînement de modèles d'IA. RegAid répond aux exigences de souveraineté des données des organisations européennes des sciences de la vie.
Pour les équipes réglementaires qui ont besoin de rapidité, de traçabilité et d'un travail défendable.
RegAid aide les équipes réglementaires à poser des questions, rédiger des réponses sourcées, comparer les exigences et identifier les lacunes dans 20M+ documents officiels de la FDA, l'EMA, Swissmedic et 10+ autres autorités. Chaque réponse traçable jusqu'à la source.
RegAid est conçu pour les responsables des affaires réglementaires, les consultants réglementaires, les responsables assurance qualité, les startups de dispositifs médicaux, les organismes de recherche sous contrat (CRO) et les équipes de conformité pharma et MedTech. Que vous prépariez une soumission 510(k), naviguiez le marquage CE selon l'EU MDR, compariez les lignes directrices ICH entre juridictions ou rédigiez des soumissions Swissmedic, RegAid vous permet d'interroger, de rédiger et de citer à partir de sources officielles en quelques secondes au lieu d'heures de recherche manuelle.
ou
En continuant, vous acceptez la Politique de confidentialité et les Conditions d'utilisation.
Pour le marquage CE, le dossier technique doit couvrir l'annexe II et les éléments post-commercialisation de l'annexe III eur-lex.europa.eu. Les principaux écarts sont les suivants :
Le dossier technique n'est pas encore prêt pour le marquage CE. Les sections manquantes des annexes II et III doivent être complétées ensuite eur-lex.europa.eu.
Assistant
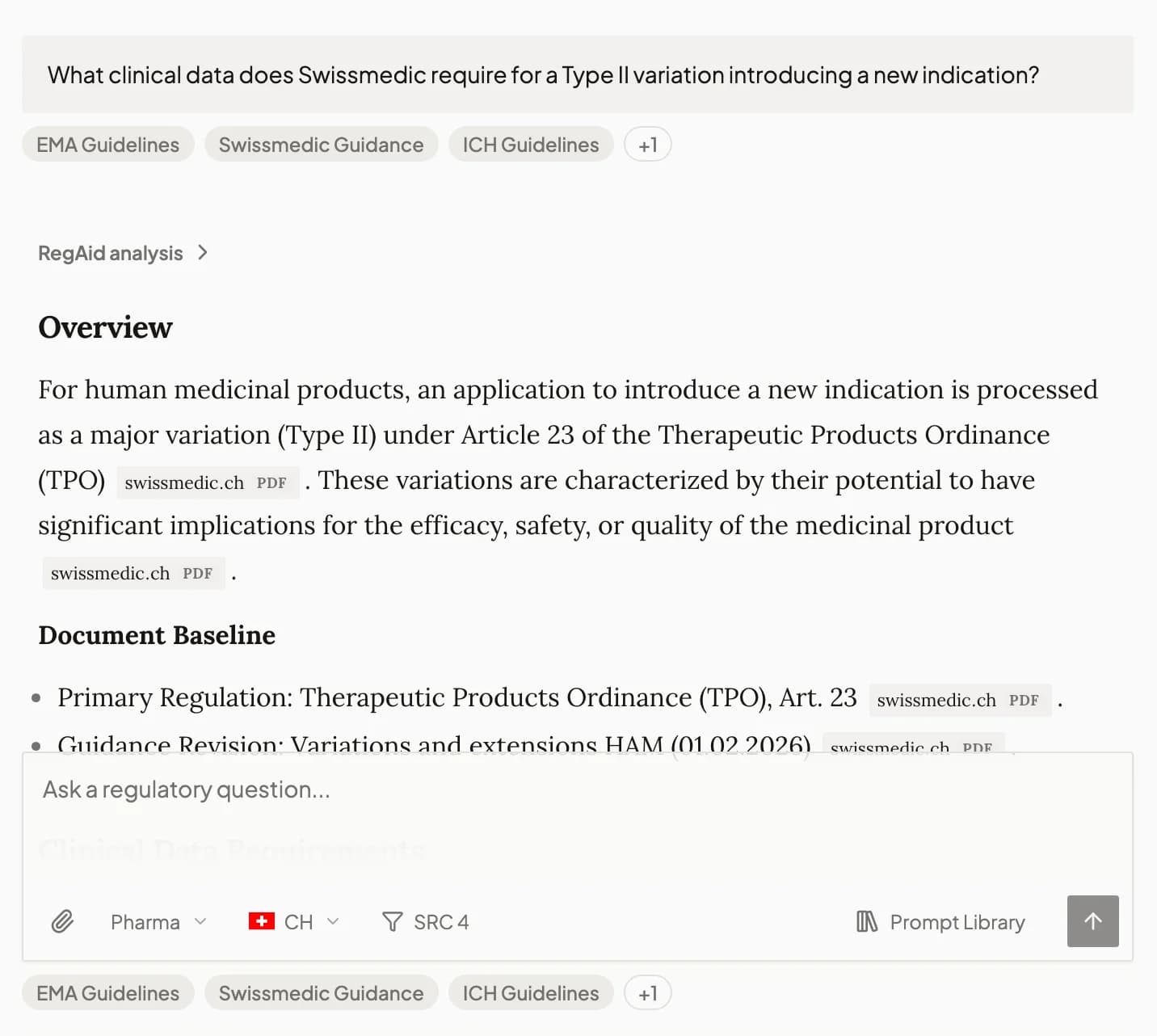
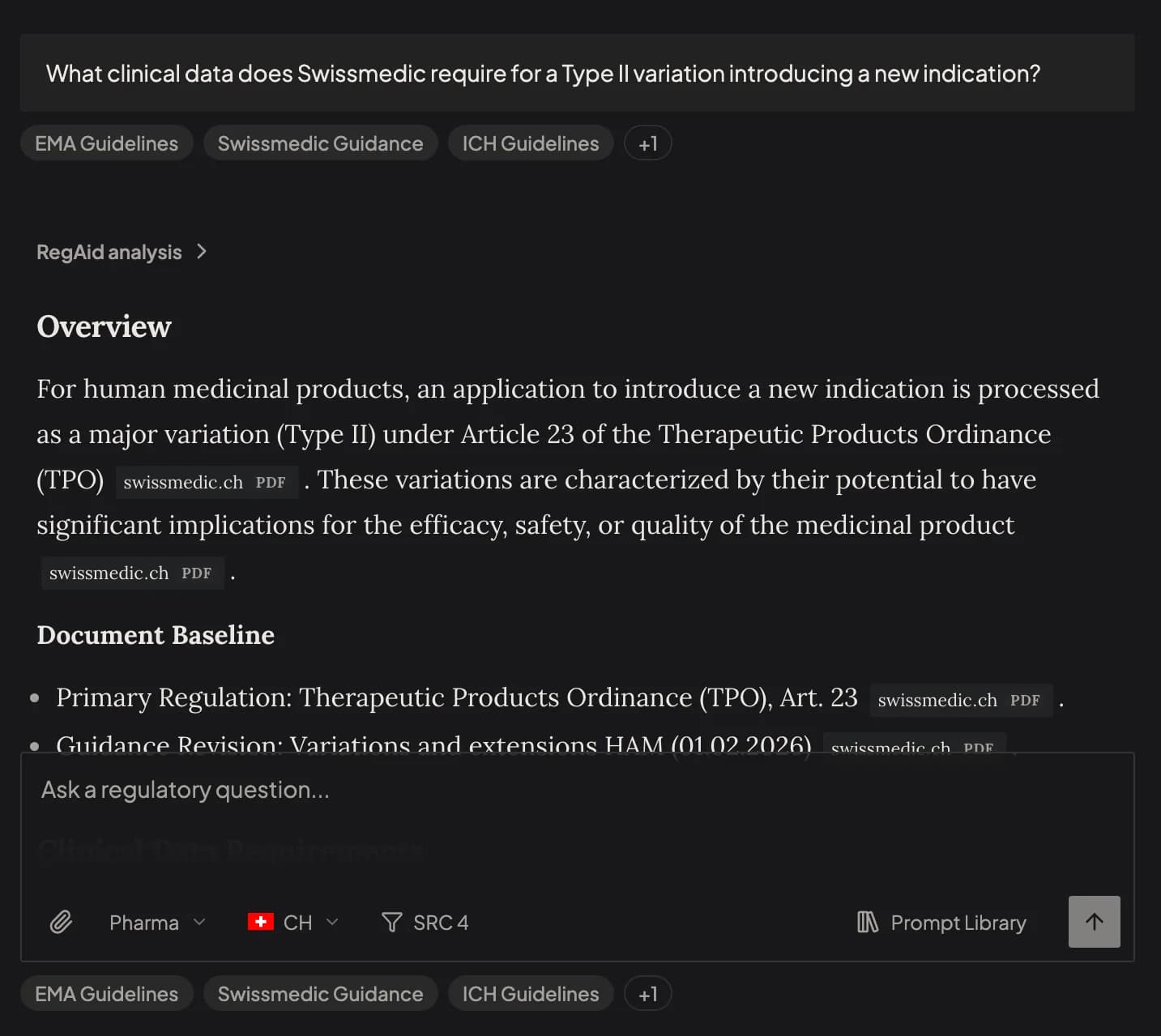

Éditeur




Analyse Tabulaire




Monitoring




Word Add-in
Lignes directrices, autorisations, étiquetage, évaluations et réglementation auprès de 10+ autorités.
| Juridiction | Lignes directrices | Autorisations | Étiquetage & IFU | Évaluations | Réglementation |
|---|---|---|---|---|---|
| 🇺🇸US (FDA) | US (FDA) Lignes directrices: Covered | US (FDA) Autorisations: Covered | US (FDA) Étiquetage & IFU: Covered | US (FDA) Évaluations: Covered | US (FDA) Réglementation: Covered |
| 🇪🇺UE (EMA) | UE (EMA) Lignes directrices: Covered | UE (EMA) Autorisations: Covered | UE (EMA) Étiquetage & IFU: Covered | UE (EMA) Évaluations: Covered | UE (EMA) Réglementation: Covered |
| 🇨🇭Suisse | Suisse Lignes directrices: Covered | Suisse Autorisations: Covered | Suisse Étiquetage & IFU: Covered | Suisse Évaluations: Covered | Suisse Réglementation: Covered |
| 🇨🇦Canada | Canada Lignes directrices: Covered | Canada Autorisations: Covered | Canada Étiquetage & IFU: Covered | Canada Évaluations: Covered | Canada Réglementation: Covered |
| 🇬🇧UK (MHRA) | UK (MHRA) Lignes directrices: Covered | UK (MHRA) Autorisations: Covered | UK (MHRA) Étiquetage & IFU: Covered | UK (MHRA) Évaluations: Covered | UK (MHRA) Réglementation: Covered |
| 🇯🇵🇨🇳🇮🇳+ autres | + autres Lignes directrices: Covered | + autres Autorisations: Covered | + autres Étiquetage & IFU: Covered | + autres Évaluations: Covered | + autres Réglementation: Covered |
| 🌐ICH | ICH Lignes directrices: Covered | ICH Autorisations: Not applicable | ICH Étiquetage & IFU: Not applicable | ICH Évaluations: Not applicable | ICH Réglementation: Not applicable |
Recherchez dans toute réglementation. Obtenez des réponses citées.
Accès complet, facturation mensuelle
20 recherches gratuites · 30 jours · sans carte de crédit
Accès complet, facturation annuelle
20 recherches gratuites · 30 jours · sans carte de crédit
Pour les équipes aux besoins avancés
Pharma et MedTech dans 10 juridictions. Lignes directrices, autorisations, données dispositifs, informations de prescription et rapports d'évaluation de FDA, EMA, Swissmedic, Health Canada, MHRA, ICH et plus.
RegAid ne répond qu'à partir de sources réglementaires officielles. Chaque réponse est citée avec le document original. Les outils IA généraux n'ont pas de couverture réglementaire, pas de citations, pas de grilles de comparaison et pas de surveillance des changements. Si RegAid ne trouve pas de source fiable, il vous le dit au lieu de deviner.
Chaque réponse inclut des citations cliquables vers le document source. Pas de source, pas de réponse.
Oui. Posez des questions de workflow comme « Quelles preuves cliniques sont requises pour un CER de Classe III sous MDR ? » et obtenez une réponse structurée et citée. Utilisez les grilles de comparaison pour cartographier les exigences entre juridictions pour tout type de soumission.
Oui. Téléchargez votre documentation technique, protocoles ou soumissions. RegAid les compare aux exigences officielles et vous montre exactement où sont les écarts, avec citations à la source.
Oui. Créez des grilles de comparaison sur toutes les juridictions, téléchargez vos propres documents pour identifier les lacunes de conformité, et laissez l'assistant IA remplir chaque cellule avec des réponses citées.
Hébergé en Suisse (GCP Zurich). Conforme RGPD + nLPD. Données jamais utilisées pour l'entraînement IA.
CHF 1'990/siège/an (ou CHF 199/siège/mois). Essai gratuit, aucune carte de crédit requise.
Oui. Inscrivez-vous et commencez à rédiger immédiatement, sans carte de crédit.
Oui. RegAid offre une expérience proche d’une vraie application sur ordinateur et mobile. Vous pouvez l’installer dans Chrome ou Edge depuis la barre d’adresse, ou l’ajouter depuis Safari avec Ajouter à l’écran d’accueil (iOS) ou Ajouter au Dock (macOS).