Ospitato in Svizzera. Conforme GDPR + LPD.
RegAid è interamente ospitato in Svizzera ed è conforme sia al Regolamento Generale sulla Protezione dei Dati (GDPR) dell'UE sia alla Legge federale svizzera sulla Protezione dei Dati (LPD). Tutti i dati vengono elaborati e archiviati in data center svizzeri. I dati degli utenti non vengono mai utilizzati per l'addestramento di modelli di IA. RegAid supporta i requisiti di sovranità dei dati delle organizzazioni europee nel settore delle scienze della vita.
Il lavoro regolatorio, fondato sulle fonti.
Per team regolatori che hanno bisogno di velocità, tracciabilità e lavoro difendibile.
RegAid aiuta i team regolatori a porre domande, redigere risposte con fonti, confrontare i requisiti e identificare le lacune in oltre 20M di documenti ufficiali di FDA, EMA, Swissmedic e altre 10 autorità. Ogni risposta tracciabile alla fonte.
RegAid è progettato per responsabili degli affari regolatori, consulenti regolatori, responsabili della garanzia qualità, startup di dispositivi medici, organizzazioni di ricerca a contratto (CRO) e team di conformità pharma e MedTech. Che stiate preparando una sottomissione 510(k), navigando la marcatura CE secondo l'EU MDR, confrontando le linee guida ICH tra giurisdizioni o redigendo sottomissioni Swissmedic, RegAid vi consente di chiedere, redigere e citare da fonti ufficiali in pochi secondi anziché in ore di ricerca manuale.
Per la marcatura CE, il fascicolo tecnico deve coprire l'Allegato II e gli elementi post-market dell'Allegato III eur-lex.europa.eu. Le principali lacune sono:
- Struttura dell'Allegato II: La descrizione del dispositivo e la destinazione d'uso sono presenti, ma il fascicolo ha ancora bisogno di una struttura dell'Allegato II più chiara eur-lex.europa.eu
- Evidenze GSPR: La bozza include descrizione del prodotto e IFU, ma checklist GSPR, collegamento al rischio ed evidenze di verifica sono incomplete
- Prontezza per l'Allegato III: PMS, pianificazione PMCF e procedure di vigilanza devono ancora essere documentate nel fascicolo CE eur-lex.europa.eu
Il fascicolo tecnico non è ancora pronto per la marcatura CE. Le sezioni mancanti dell'Allegato II e III dovrebbero essere completate come prossimo passo eur-lex.europa.eu.
Giurisdizione
Globale
Stati Uniti (FDA)
Unione europea (EMA)
Svizzera (Swissmedic)
Regno Unito (MHRA)
Canada (Health Canada)
Cina
Nigeria (NAFDAC)
Sudafrica (SAHPRA)
India (CDSCO)
Giappone (PMDA)
Fonti
Linee guida FDA
Approvazioni dispositivi FDA
Linee guida EMA
Linee guida Swissmedic
Linee guida CDE
Linee guida ICH
eCFR
CRLs
Linee guida MHRA
Linee guida Health Canada
Linee guida NAFDAC
Linee guida SAHPRA
Linee guida CDSCO
Linee guida PMDA
Analisi
Analisi della domanda
Pianificazione della strategia di ricerca
Ricerca nelle fonti
Lettura di 12 fonti
Redazione di una risposta con fonti
Preparazione di 4 citazioni
Assistente
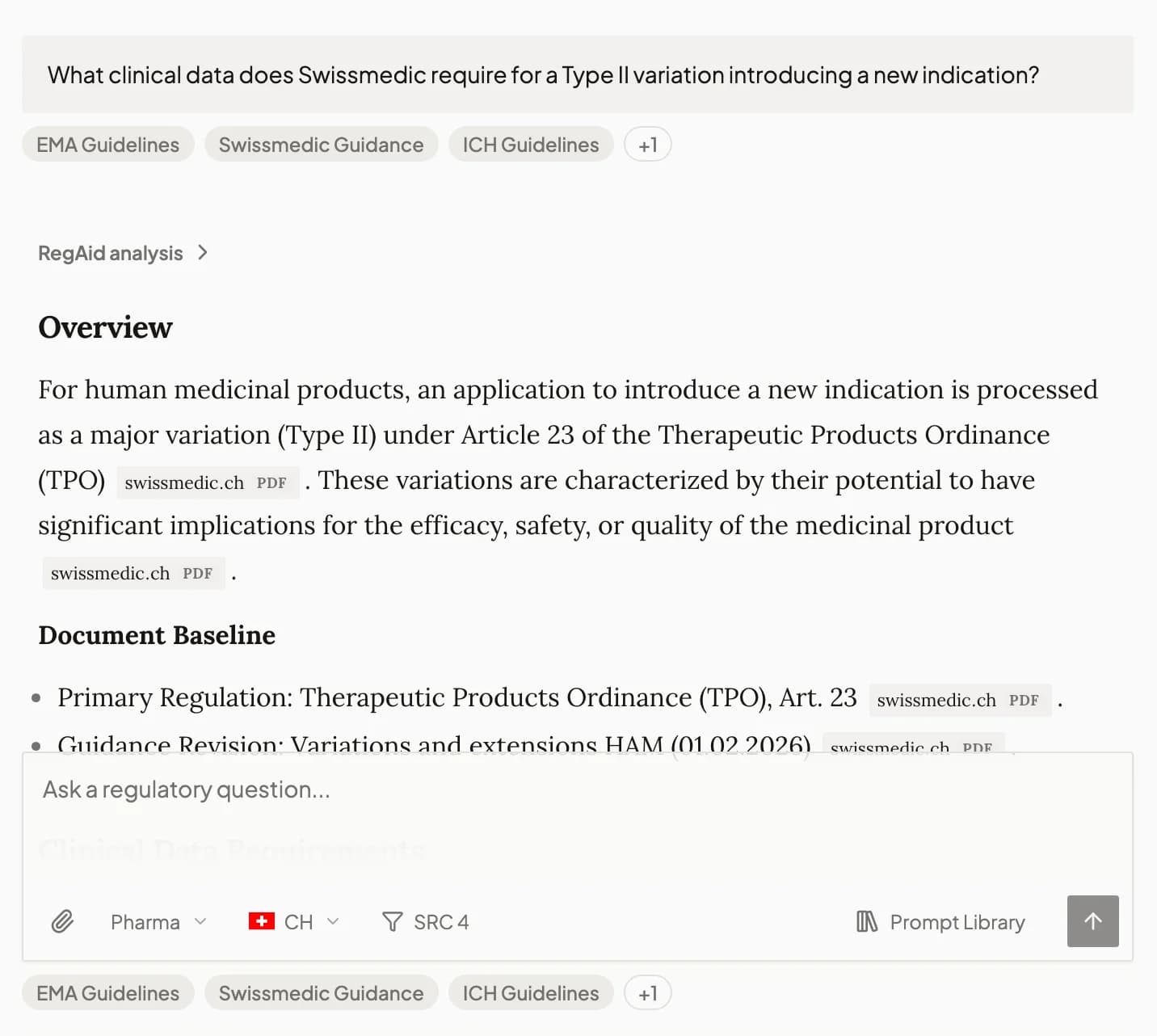
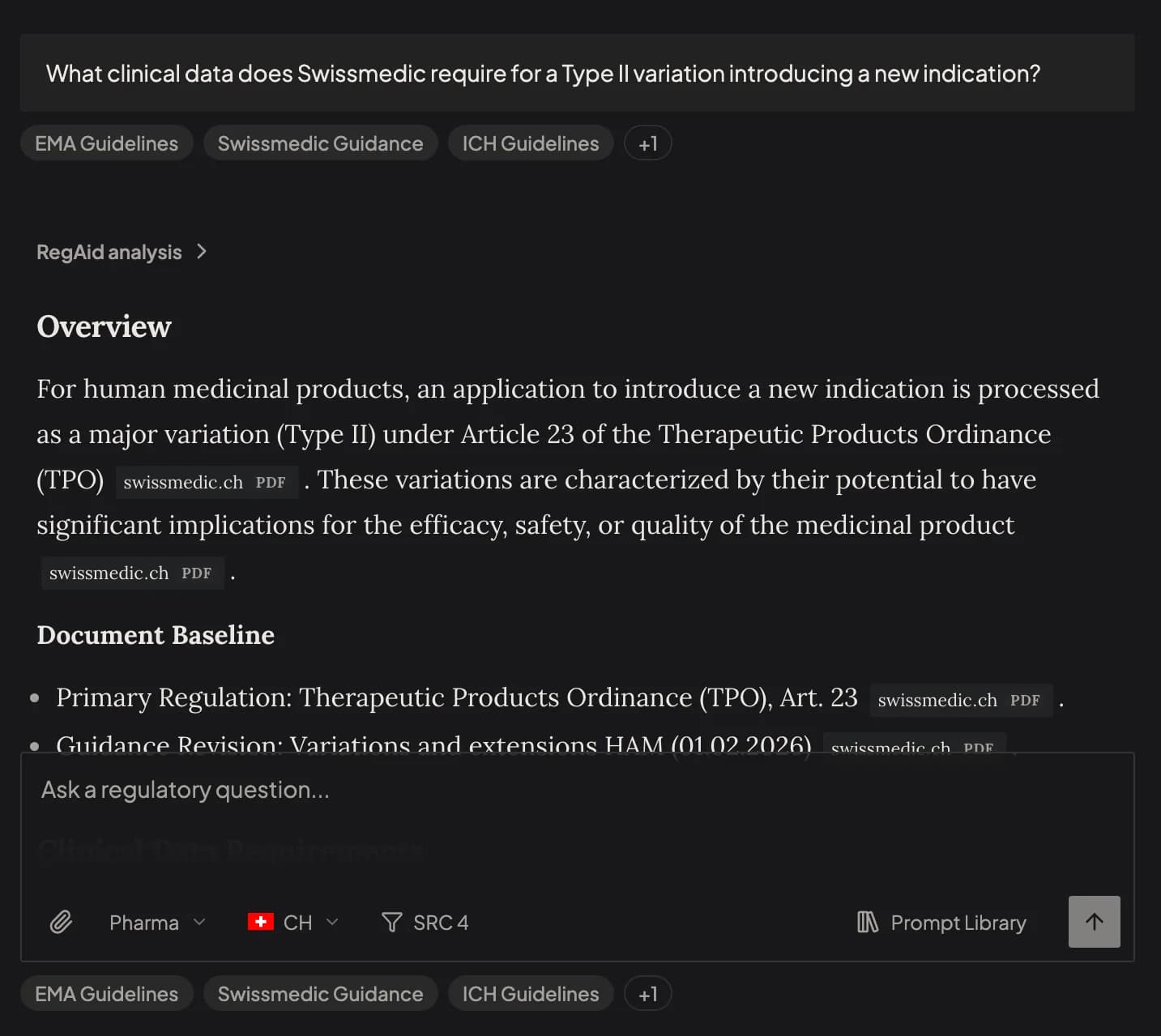
Poni qualsiasi domanda regolatoria
- Una domanda. RegAid redige, verifica e cita su oltre 10 autorità.
- Ogni risposta tracciabile fino alla sezione esatta nella fonte
- Dati in tempo reale dalle fonti ufficiali. Autorizzazioni 510(k), approvazioni di farmaci, richiami e aggiornamenti in tempo reale.
- Caricate il vostro documento. Vedete dove è carente.
- Continuate la conversazione. RegAid ricorda il vostro contesto.

Editor
Redigi con sicurezza. Rivedi inline.
- Crea sezioni CER, bozze di risposta alle autorità e memo di strategia regolatoria con citazioni allegate mentre scrivi.
- Bozze con versioning e cronologia completa. Ogni revisione auditabile.
- Pannello evidenze inline con click di accesso al paragrafo sorgente esatto.
- Flusso di revisione: assegna, commenta, approva. Le modifiche tracciate si esportano in modo pulito nel tuo QMS.
- Trasforma qualsiasi risposta dell'Assistente in un documento bozza con un clic.




Analisi Tabellare
Confronto tra giurisdizioni e analisi delle lacune.
- Costruisci griglie di confronto tra giurisdizioni (FDA vs EMA vs Swissmedic vs MHRA) in pochi secondi.
- Esegui valutazioni delle lacune: carica il tuo dossier, vedi dove non soddisfa le aspettative di ciascuna autorità, con citazioni.
- Mappa la classificazione dei dispositivi, le evidenze cliniche o i requisiti di etichettatura tra mercati.
- Ogni cella traccia al suo paragrafo sorgente.
- Esporta in Word, PDF o CSV quando pronto per la revisione.




Monitoring
Tracciate i cambiamenti regolatori con alert citati.
- Scegli un argomento, una giurisdizione e le fonti. Configurato in pochi secondi.
- Consegnato via e-mail o notifica push. Digest giornaliero o settimanale.
- Nuove linee guida pubblicate? Lo saprete per primi, con citazioni.
- Condividete i watcher con il vostro team. Tutti tracciano gli stessi aggiornamenti.
- Ogni aggiornamento rimanda alla fonte. Cliccate per verificare.




Word Add-in
Valida, riscrivi e cita. Direttamente in Word.
- Selezionate un paragrafo qualsiasi e verificate se è supportato dalle linee guida ufficiali, con un verdetto chiaro e prove citate
- Trovate la citazione per qualsiasi affermazione e inseritela inline con un clic
- Inserite una tabella comparativa tra giurisdizioni direttamente nel vostro documento
- Riscrivete il testo normativo con revisione delle modifiche affinché i revisori vedano esattamente cosa è cambiato
- Revisione contestuale che si adatta automaticamente al documento regolatorio su cui state lavorando
Ogni giurisdizione principale. Un'unica area di lavoro.
Linee guida, approvazioni, etichette, valutazioni e regolamenti presso 10+ autorità.
| Giurisdizione | Linee guida | Approvazioni | Etichette e IFU | Valutazioni | Regolamenti |
|---|---|---|---|---|---|
| 🇺🇸US (FDA) | US (FDA) Linee guida: Covered | US (FDA) Approvazioni: Covered | US (FDA) Etichette e IFU: Covered | US (FDA) Valutazioni: Covered | US (FDA) Regolamenti: Covered |
| 🇪🇺UE (EMA) | UE (EMA) Linee guida: Covered | UE (EMA) Approvazioni: Covered | UE (EMA) Etichette e IFU: Covered | UE (EMA) Valutazioni: Covered | UE (EMA) Regolamenti: Covered |
| 🇨🇭Svizzera | Svizzera Linee guida: Covered | Svizzera Approvazioni: Covered | Svizzera Etichette e IFU: Covered | Svizzera Valutazioni: Covered | Svizzera Regolamenti: Covered |
| 🇨🇦Canada | Canada Linee guida: Covered | Canada Approvazioni: Covered | Canada Etichette e IFU: Covered | Canada Valutazioni: Covered | Canada Regolamenti: Covered |
| 🇬🇧UK (MHRA) | UK (MHRA) Linee guida: Covered | UK (MHRA) Approvazioni: Covered | UK (MHRA) Etichette e IFU: Covered | UK (MHRA) Valutazioni: Covered | UK (MHRA) Regolamenti: Covered |
| 🇯🇵🇨🇳🇮🇳+ altri | + altri Linee guida: Covered | + altri Approvazioni: Covered | + altri Etichette e IFU: Covered | + altri Valutazioni: Covered | + altri Regolamenti: Covered |
| 🌐ICH | ICH Linee guida: Covered | ICH Approvazioni: Not applicable | ICH Etichette e IFU: Not applicable | ICH Valutazioni: Not applicable | ICH Regolamenti: Not applicable |
Prezzi
Cerca qualsiasi regolamento. Ottieni risposte citate.
Mensile
Accesso completo, fatturazione mensile
CHF 199/ postazione / mese
20 ricerche gratuite · 30 giorni · senza carta di credito
- Ricerche illimitate con risposte citate
- Carica e confronta i tuoi documenti con fonti ufficiali
- Analisi delle lacune e confronto tra giurisdizioni
- Monitoraggio dei cambiamenti normativi con avvisi citati
- Spazi di lavoro di team con accesso basato sui ruoli
- Sessioni condivisibili ed esportazione CSV
- Oltre 10 autorità regolatorie coperte
Annuale
Accesso completo, fatturazione annuale
CHF 1'990/ postazione / anno
20 ricerche gratuite · 30 giorni · senza carta di credito
- Tutto nel piano Mensile
- 2 mesi gratis (risparmi CHF 398)
- Supporto prioritario
Enterprise
Per team con esigenze avanzate
Personalizzato
- Tutto nel piano Annuale
- Integrazioni di fonti personalizzate
- Onboarding dedicato
- Supporto prioritario
- Prezzi per volume
Domande frequenti
01
Cosa copre RegAid?
Pharma e MedTech in 10 giurisdizioni. Linee guida, approvazioni farmaci, autorizzazioni dispositivi, informazioni prescrittive e rapporti di valutazione da FDA, EMA, Swissmedic, Health Canada, MHRA, ICH e altro.
02
In cosa si differenzia RegAid da ChatGPT o strumenti IA generici?
RegAid risponde esclusivamente da fonti regolatorie ufficiali. Ogni risposta è citata con il documento originale. Gli strumenti IA generici non hanno copertura di fonti regolatorie, nessuna citazione, nessuna griglia di confronto e nessun monitoraggio dei cambiamenti. Se RegAid non trova una fonte affidabile, ve lo dice invece di inventare.
03
Quanto sono accurate le risposte?
Ogni risposta include citazioni cliccabili al documento fonte. Nessuna fonte, nessuna risposta.
04
RegAid supporta workflow CER, PMCF, PSUR, 510(k) e altri?
Sì. Ponete domande sui workflow come «Quali evidenze cliniche sono richieste per un CER di Classe III sotto MDR?» e ottenete una risposta strutturata e citata. Usate le griglie di confronto per mappare i requisiti tra giurisdizioni per qualsiasi tipo di sottomissione.
05
Posso caricare i miei documenti e confrontarli con le normative?
Sì. Caricate la vostra documentazione tecnica, protocolli o sottomissioni. RegAid li confronta con i requisiti ufficiali e vi mostra esattamente dove sono le lacune, con citazioni alla fonte.
06
Posso confrontare le normative e identificare le lacune?
Sì. Crea griglie di confronto su qualsiasi giurisdizione, carica i tuoi documenti per identificare le lacune di conformità, e lascia che l'assistente IA riempia ogni cella con risposte citate.
07
Dove vengono archiviati i miei dati?
Ospitato in Svizzera (GCP Zurigo). Conforme GDPR + nLPD. Dati mai usati per addestramento IA.
08
Quanto costa RegAid?
CHF 1'990/posto/anno (o CHF 199/posto/mese). Prova gratuita, nessuna carta di credito richiesta.
09
Posso provarlo prima?
Sì. Registrati e inizia subito a redigere, nessuna carta di credito richiesta.
10
Posso installare RegAid come app su desktop o mobile?
Sì. RegAid offre un’esperienza simile a una vera app su desktop e mobile. Puoi installarla in Chrome o Edge dalla barra degli indirizzi, oppure aggiungerla da Safari con Aggiungi alla schermata Home (iOS) o Aggiungi al Dock (macOS).






