Alojado en Suiza. Conforme con GDPR + FADP.
RegAid está alojado íntegramente en Suiza y cumple tanto con el Reglamento General de Protección de Datos (GDPR) de la UE como con la Ley Federal Suiza de Protección de Datos (FADP). Todos los datos se procesan y almacenan en centros de datos suizos. Los datos de los usuarios nunca se utilizan para el entrenamiento de modelos de IA. RegAid cumple con los requisitos de soberanía de datos de las organizaciones europeas de ciencias de la vida.
Trabajo regulatorio, basado en fuentes.
Para equipos regulatorios que necesitan velocidad, trazabilidad y trabajo defendible.
RegAid ayuda a los equipos regulatorios a hacer preguntas, redactar respuestas citadas, comparar requisitos e identificar brechas en más de 20M de documentos oficiales de FDA, EMA, Swissmedic y otras 10+ autoridades. Cada respuesta rastreable hasta la fuente.
RegAid está diseñado para responsables de asuntos regulatorios, consultores regulatorios, responsables de aseguramiento de calidad, startups de dispositivos médicos, organizaciones de investigación por contrato (CROs) y equipos de cumplimiento de farma y MedTech. Ya sea que esté preparando una presentación 510(k), gestionando el marcado CE según la EU MDR, comparando directrices ICH entre jurisdicciones o redactando presentaciones para Swissmedic, RegAid le permite preguntar, redactar y citar desde fuentes oficiales en segundos en lugar de horas de investigación manual.
Para el marcado CE, el expediente técnico debe cubrir el Anexo II y los elementos poscomercialización del Anexo III eur-lex.europa.eu. Las principales brechas son:
- Estructura del Anexo II: La descripción del dispositivo y el uso previsto están presentes, pero el expediente aún necesita una estructura del Anexo II más clara eur-lex.europa.eu
- Evidencia GSPR: El borrador incluye descripción del producto e IFU, pero la lista GSPR, la vinculación de riesgos y la evidencia de verificación están incompletas
- Preparación para el Anexo III: La PMS, la planificación PMCF y los procedimientos de vigilancia aún deben documentarse para el expediente CE eur-lex.europa.eu
El expediente técnico aún no está listo para CE. Las secciones faltantes del Anexo II y III deberían completarse a continuación eur-lex.europa.eu.
Jurisdicción
Global
Estados Unidos (FDA)
Unión Europea (EMA)
Suiza (Swissmedic)
Reino Unido (MHRA)
Canadá (Health Canada)
China
Nigeria (NAFDAC)
Sudáfrica (SAHPRA)
India (CDSCO)
Japón (PMDA)
Fuentes
Guías FDA
Aprobaciones de dispositivos FDA
Directrices EMA
Guías Swissmedic
Orientaciones CDE
Directrices ICH
eCFR
CRLs
Guías MHRA
Guías de Health Canada
Orientaciones NAFDAC
Orientaciones SAHPRA
Orientaciones CDSCO
Orientaciones PMDA
Análisis
Analizando la pregunta
Planificando la estrategia de recuperación
Buscando en las fuentes
Leyendo 12 fuentes
Redactando una respuesta fundamentada
Preparando 4 citas
Asistente
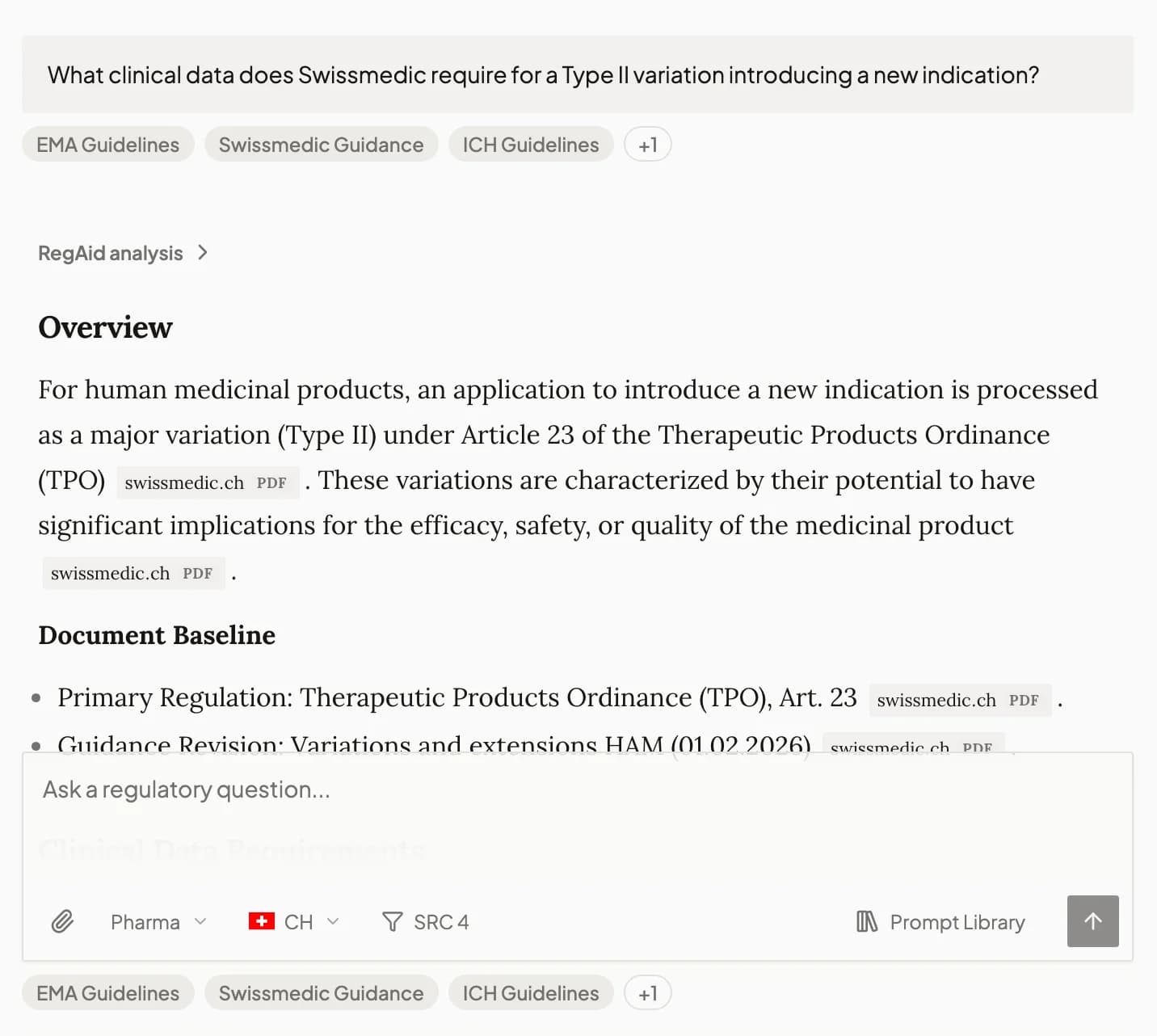
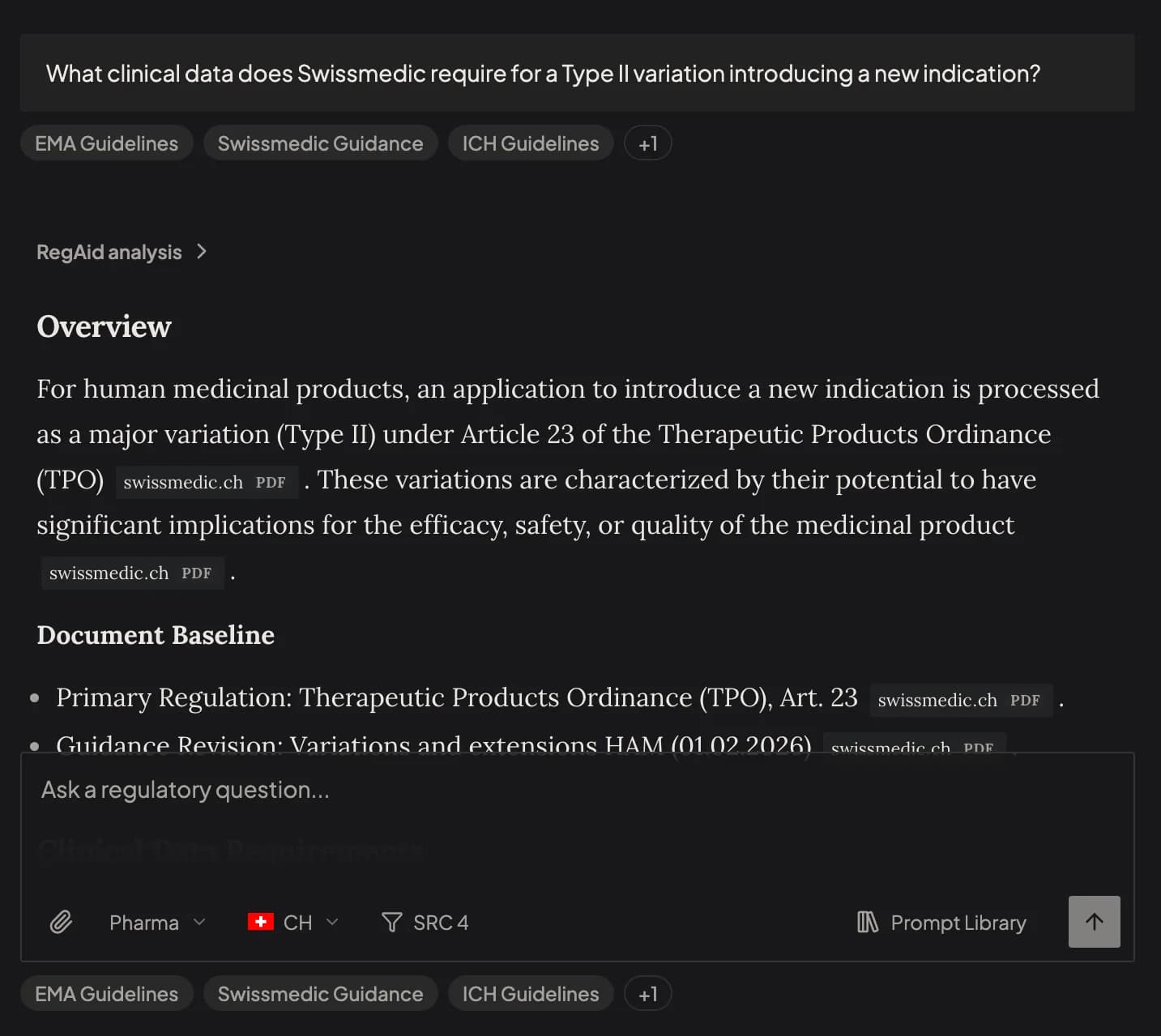
Haga cualquier pregunta regulatoria
- Una pregunta. RegAid redacta, verifica y cita en más de 10 autoridades.
- Cada respuesta rastreable hasta la sección exacta en la fuente
- Datos en vivo de fuentes oficiales. Autorizaciones 510(k), aprobaciones de medicamentos, retiros y actualizaciones en tiempo real.
- Sube tu documento. Mira dónde se queda corto.
- Continúa la conversación. RegAid recuerda tu contexto.

Editor
Redacte con confianza. Revise en línea.
- Cree secciones de CER, borradores de respuestas a autoridades y memos de estrategia regulatoria con citas adjuntas mientras escribe.
- Borradores con versiones e historial completo. Cada revisión auditable.
- Panel de evidencia en línea con acceso directo al párrafo de origen exacto.
- Flujo de revisión: asignar, comentar, aprobar. Los cambios rastreados se exportan limpiamente a su QMS.
- Convierta cualquier respuesta del Asistente en un borrador de documento con un clic.




Análisis Tabular
Comparación entre jurisdicciones y análisis de brechas.
- Construya cuadrículas de comparación entre jurisdicciones (FDA vs EMA vs Swissmedic vs MHRA) en segundos.
- Ejecute evaluaciones de brechas: cargue su dosier, vea dónde no cumple con las expectativas de cada autoridad, con citas.
- Mapee clasificación de dispositivos, evidencia clínica o requisitos de etiquetado entre mercados.
- Cada celda rastrea hasta su párrafo fuente.
- Exporte a Word, PDF o CSV cuando esté listo para revisión.




Monitoring
Rastree el cambio regulatorio con alertas citadas.
- Elija un tema, jurisdicción y fuentes. Configurado en segundos.
- Entregado por correo electrónico o notificación push. Resumen diario o semanal.
- ¿Nuevas directrices publicadas? Lo sabrá primero, con citas.
- Comparta los watchers con su equipo. Todos rastrean las mismas actualizaciones.
- Cada actualización enlaza a la fuente. Haga clic para verificar.




Word Add-in
Valide, reescriba y cite. Directamente en Word.
- Seleccione cualquier párrafo y vea si está respaldado por las directrices oficiales, con un veredicto claro y evidencia citada
- Encuentre la cita para cualquier afirmación e insértela en línea con un clic
- Inserte una tabla comparativa entre jurisdicciones directamente en su documento
- Reescriba texto regulatorio con control de cambios para que los revisores vean exactamente qué cambió
- Revisión contextual que se adapta automáticamente al documento regulatorio en el que está trabajando
Cada jurisdicción principal. Un espacio de trabajo.
Directrices, aprobaciones, etiquetas, evaluaciones y reglamentación de 10+ autoridades.
| Jurisdicción | Directrices | Aprobaciones | Etiquetas e IFU | Evaluaciones | Reglamentación |
|---|---|---|---|---|---|
| 🇺🇸US (FDA) | US (FDA) Directrices: Covered | US (FDA) Aprobaciones: Covered | US (FDA) Etiquetas e IFU: Covered | US (FDA) Evaluaciones: Covered | US (FDA) Reglamentación: Covered |
| 🇪🇺UE (EMA) | UE (EMA) Directrices: Covered | UE (EMA) Aprobaciones: Covered | UE (EMA) Etiquetas e IFU: Covered | UE (EMA) Evaluaciones: Covered | UE (EMA) Reglamentación: Covered |
| 🇨🇭Suiza | Suiza Directrices: Covered | Suiza Aprobaciones: Covered | Suiza Etiquetas e IFU: Covered | Suiza Evaluaciones: Covered | Suiza Reglamentación: Covered |
| 🇨🇦Canadá | Canadá Directrices: Covered | Canadá Aprobaciones: Covered | Canadá Etiquetas e IFU: Covered | Canadá Evaluaciones: Covered | Canadá Reglamentación: Covered |
| 🇬🇧UK (MHRA) | UK (MHRA) Directrices: Covered | UK (MHRA) Aprobaciones: Covered | UK (MHRA) Etiquetas e IFU: Covered | UK (MHRA) Evaluaciones: Covered | UK (MHRA) Reglamentación: Covered |
| 🇯🇵🇨🇳🇮🇳+ otros | + otros Directrices: Covered | + otros Aprobaciones: Covered | + otros Etiquetas e IFU: Covered | + otros Evaluaciones: Covered | + otros Reglamentación: Covered |
| 🌐ICH | ICH Directrices: Covered | ICH Aprobaciones: Not applicable | ICH Etiquetas e IFU: Not applicable | ICH Evaluaciones: Not applicable | ICH Reglamentación: Not applicable |
Precios
Busque cualquier regulación. Obtenga respuestas citadas.
Mensual
Acceso completo, facturación mensual
CHF 199/ puesto / mes
20 búsquedas gratis · 30 días · sin tarjeta de crédito
- Búsquedas ilimitadas con respuestas citadas
- Carga y cruza tus propios documentos con fuentes oficiales
- Análisis de brechas y comparación entre jurisdicciones
- Monitoreo de cambios regulatorios con alertas citadas
- Espacios de trabajo en equipo con acceso por roles
- Sesiones compartibles y exportación en CSV
- Más de 10 autoridades regulatorias cubiertas
Anual
Acceso completo, facturación anual
CHF 1'990/ puesto / año
20 búsquedas gratis · 30 días · sin tarjeta de crédito
- Todo en Mensual
- 2 meses gratis (ahorre CHF 398)
- Soporte prioritario
Enterprise
Para equipos con necesidades avanzadas
Personalizado
- Todo en Anual
- Integraciones de fuentes personalizadas
- Onboarding dedicado
- Soporte prioritario
- Precios por volumen
Preguntas frecuentes
01
¿Qué cubre RegAid?
Pharma y MedTech en 10 jurisdicciones. Directrices, aprobaciones de medicamentos, autorizaciones de dispositivos, información de prescripción e informes de evaluación de FDA, EMA, Swissmedic, Health Canada, MHRA, ICH y más.
02
¿En qué se diferencia RegAid de ChatGPT o herramientas de IA generales?
RegAid solo responde a partir de fuentes regulatorias oficiales. Cada respuesta está citada con el documento original. Las herramientas de IA generales no tienen cobertura de fuentes regulatorias, ni citas, ni cuadrículas de comparación, ni monitoreo de cambios. Si RegAid no encuentra una fuente fiable, se lo dice en lugar de adivinar.
03
¿Qué tan precisas son las respuestas?
Cada respuesta incluye citas clicables al documento fuente. Sin fuente, sin respuesta.
04
¿RegAid soporta flujos de trabajo CER, PMCF, PSUR, 510(k) y otros?
Sí. Haga preguntas de flujo de trabajo como «¿Qué evidencia clínica se requiere para un CER de Clase III bajo MDR?» y obtenga una respuesta estructurada y citada. Use cuadrículas de comparación para mapear requisitos entre jurisdicciones para cualquier tipo de presentación.
05
¿Puedo subir mis propios documentos y compararlos con las regulaciones?
Sí. Suba su documentación técnica, protocolos o presentaciones. RegAid los compara con los requisitos oficiales y le muestra exactamente dónde están las brechas, con citas a la fuente.
06
¿Puedo comparar regulaciones e identificar brechas?
Sí. Crea cuadrículas de comparación en cualquier jurisdicción, sube tus propios documentos para identificar brechas de cumplimiento, y deja que el asistente de IA llene cada celda con respuestas citadas.
07
¿Dónde se almacenan mis datos?
Alojado en Suiza (GCP Zúrich). Conforme con GDPR + FADP. Datos nunca usados para entrenar IA.
08
¿Cuánto cuesta RegAid?
CHF 1.990/puesto/año (o CHF 199/puesto/mes). Prueba gratuita, sin tarjeta de crédito.
09
¿Puedo probarlo primero?
Sí. Regístrese y empiece a redactar de inmediato, sin tarjeta de crédito.
10
¿Puedo instalar RegAid como aplicación en escritorio o móvil?
Sí. RegAid funciona como una aplicación real en escritorio y móvil. Puedes instalarla en Chrome o Edge desde la barra de direcciones, o añadirla desde Safari con Añadir a pantalla de inicio (iOS) o Añadir al Dock (macOS).






