oder
Mit der Fortsetzung stimmen Sie den Datenschutzerklärung und den Nutzungsbedingungen.
RegAid wird vollständig in der Schweiz gehostet und erfüllt sowohl die EU-Datenschutz-Grundverordnung (DSGVO) als auch das Schweizer Bundesgesetz über den Datenschutz (DSG). Alle Daten werden in Schweizer Rechenzentren verarbeitet und gespeichert. Nutzerdaten werden niemals für das Training von KI-Modellen verwendet. RegAid unterstützt die Anforderungen an die Datensouveränität europäischer Life-Sciences-Organisationen.
Für Regulatory-Teams, die Geschwindigkeit, Nachvollziehbarkeit und belastbare Arbeit brauchen.
RegAid hilft Regulatory-Teams, Fragen zu stellen, zitierte Antworten zu entwerfen, Anforderungen zu vergleichen und Lücken in 20M+ offiziellen Dokumenten von FDA, EMA, Swissmedic und 10+ weiteren Behörden zu identifizieren. Jede Antwort zur Quelle nachverfolgbar.
RegAid wurde entwickelt für Regulatory-Affairs-Manager, regulatorische Berater, Qualitätssicherungsleiter, Medizinprodukte-Startups, Auftragsforschungsinstitute (CROs) sowie Pharma- und MedTech-Compliance-Teams. Ob Sie eine 510(k)-Einreichung vorbereiten, die EU MDR CE-Kennzeichnung navigieren, ICH-Richtlinien über Jurisdiktionen hinweg vergleichen oder Swissmedic-Einreichungen entwerfen, RegAid lässt Sie in Sekunden aus offiziellen Quellen fragen, entwerfen und zitieren statt stundenlanger manueller Recherche.
oder
Mit der Fortsetzung stimmen Sie den Datenschutzerklärung und den Nutzungsbedingungen.
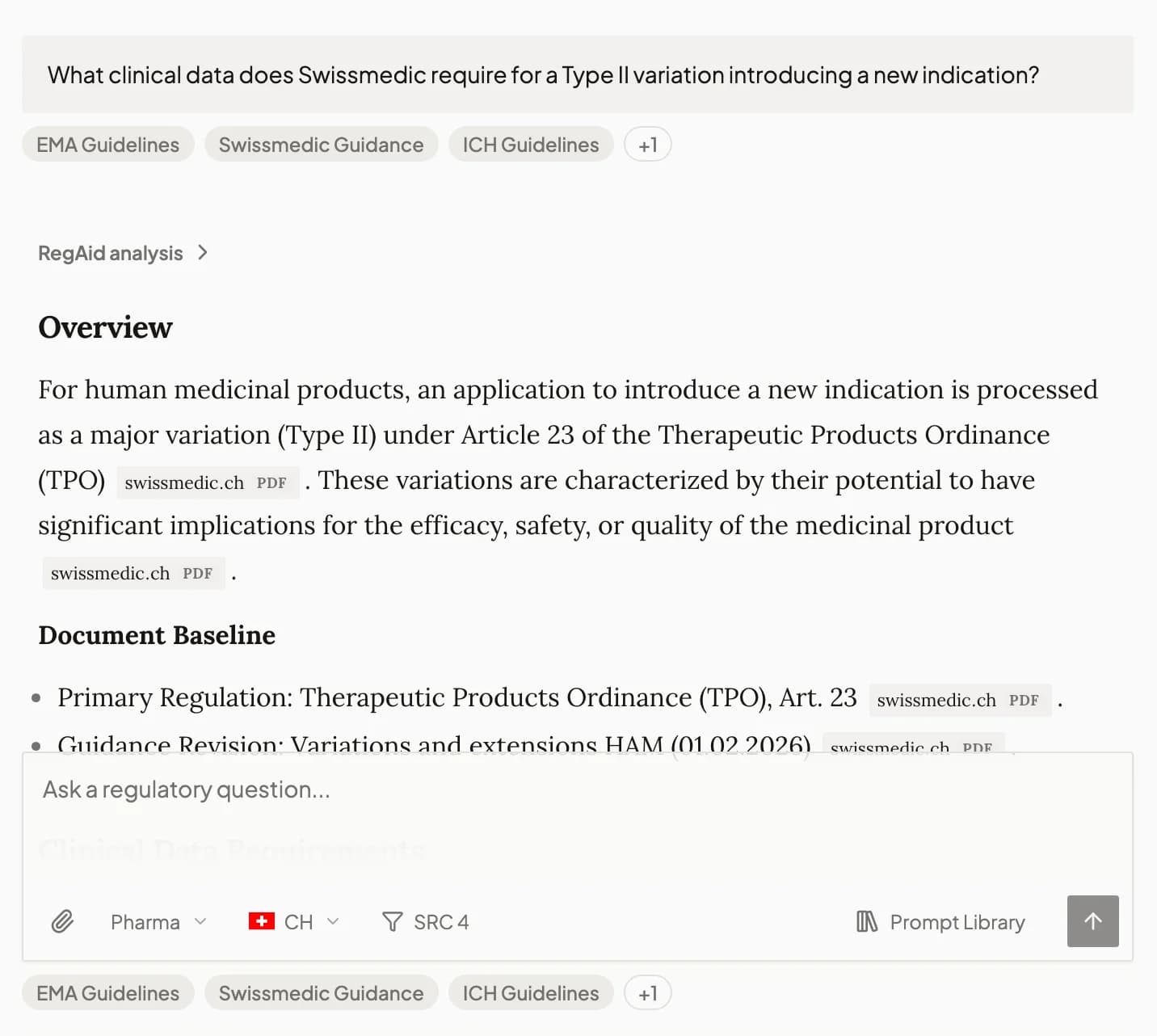
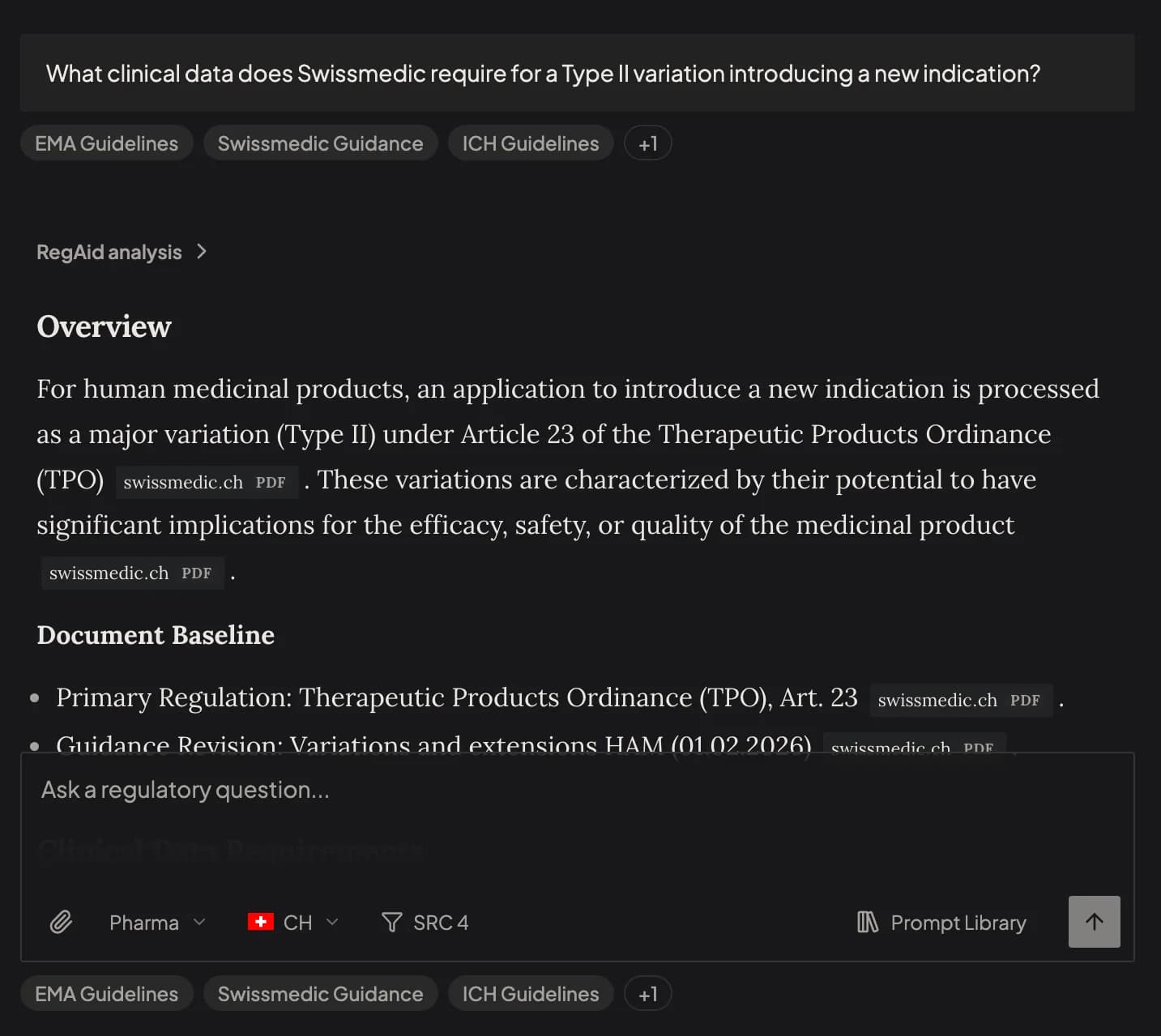
Für die CE-Kennzeichnung muss die technische Dokumentation Anhang II und die Post-Market-Elemente aus Anhang III abdecken eur-lex.europa.eu. Die wichtigsten Lücken sind:
Die technische Dokumentation ist noch nicht CE-ready. Die fehlenden Abschnitte aus Anhang II und III sollten als Nächstes ergänzt werden eur-lex.europa.eu.
Assistent

Editor




Tabellenanalyse




Monitoring




Word Add-in
Leitlinien, Zulassungen, Etiketten, Bewertungen und Vorschriften von 10+ Behörden.
| Jurisdiktion | Leitlinien | Zulassungen | Etiketten & IFUs | Bewertungen | Vorschriften |
|---|---|---|---|---|---|
| 🇺🇸US (FDA) | US (FDA) Leitlinien: Covered | US (FDA) Zulassungen: Covered | US (FDA) Etiketten & IFUs: Covered | US (FDA) Bewertungen: Covered | US (FDA) Vorschriften: Covered |
| 🇪🇺EU (EMA) | EU (EMA) Leitlinien: Covered | EU (EMA) Zulassungen: Covered | EU (EMA) Etiketten & IFUs: Covered | EU (EMA) Bewertungen: Covered | EU (EMA) Vorschriften: Covered |
| 🇨🇭Schweiz | Schweiz Leitlinien: Covered | Schweiz Zulassungen: Covered | Schweiz Etiketten & IFUs: Covered | Schweiz Bewertungen: Covered | Schweiz Vorschriften: Covered |
| 🇨🇦Kanada | Kanada Leitlinien: Covered | Kanada Zulassungen: Covered | Kanada Etiketten & IFUs: Covered | Kanada Bewertungen: Covered | Kanada Vorschriften: Covered |
| 🇬🇧UK (MHRA) | UK (MHRA) Leitlinien: Covered | UK (MHRA) Zulassungen: Covered | UK (MHRA) Etiketten & IFUs: Covered | UK (MHRA) Bewertungen: Covered | UK (MHRA) Vorschriften: Covered |
| 🇯🇵🇨🇳🇮🇳+ weitere | + weitere Leitlinien: Covered | + weitere Zulassungen: Covered | + weitere Etiketten & IFUs: Covered | + weitere Bewertungen: Covered | + weitere Vorschriften: Covered |
| 🌐ICH | ICH Leitlinien: Covered | ICH Zulassungen: Not applicable | ICH Etiketten & IFUs: Not applicable | ICH Bewertungen: Not applicable | ICH Vorschriften: Not applicable |
Jede Regulierung durchsuchen. Zitierte Antworten erhalten.
Vollzugang, monatlich abgerechnet
20 kostenlose Suchen · 30 Tage · keine Kreditkarte
Vollzugang, jährlich abgerechnet
20 kostenlose Suchen · 30 Tage · keine Kreditkarte
Für Teams mit erweiterten Anforderungen
Pharma und MedTech über 10 Jurisdiktionen. Leitlinien, Arzneimittelzulassungen, Gerätezulassungen, Fachinformationen und Bewertungsberichte von FDA, EMA, Swissmedic, Health Canada, MHRA, ICH und mehr.
RegAid antwortet ausschliesslich aus offiziellen regulatorischen Quellen. Jede Antwort ist mit dem Originaldokument zitiert. Allgemeine KI-Tools haben keine regulatorische Quellenabdeckung, keine Zitate, keine Vergleichsraster und kein Änderungsmonitoring. Wenn RegAid keine zuverlässige Quelle findet, sagt es Ihnen das, statt zu raten.
Jede Antwort enthält klickbare Zitate zum Quelldokument. Keine Quelle, keine Antwort.
Ja. Stellen Sie Workflow-Fragen wie "Welche klinischen Nachweise sind für einen Klasse-III-CER unter MDR erforderlich?" und erhalten Sie eine strukturierte, zitierte Antwort. Nutzen Sie Vergleichsraster, um Anforderungen über Jurisdiktionen hinweg für jeden Einreichungstyp abzubilden.
Ja. Laden Sie Ihre technische Dokumentation, Protokolle oder Einreichungen hoch. RegAid vergleicht sie mit den offiziellen Anforderungen und zeigt Ihnen genau, wo die Lücken sind, mit Zitaten zur Quelle.
Ja. Erstellen Sie Vergleichsraster über beliebige Jurisdiktionen, laden Sie Ihre eigenen Dokumente hoch, um Compliance-Lücken zu identifizieren, und lassen Sie den KI-Assistenten jede Zelle mit zitierten Antworten füllen.
In der Schweiz gehostet (GCP Zürich). DSGVO + DSG konform. Daten werden nie für KI-Training verwendet.
CHF 1'990/Sitz/Jahr (oder CHF 199/Sitz/Monat). Kostenlose Testversion, keine Kreditkarte nötig.
Ja. Registrieren und sofort mit dem Entwerfen beginnen, keine Kreditkarte erforderlich.
Ja. RegAid fühlt sich auf Desktop und Mobilgeräten wie eine echte App an. Sie können es in Chrome oder Edge über die Adressleiste installieren oder in Safari über „Zum Home-Bildschirm“ (iOS) bzw. „Zum Dock hinzufügen“ (macOS) hinzufügen.